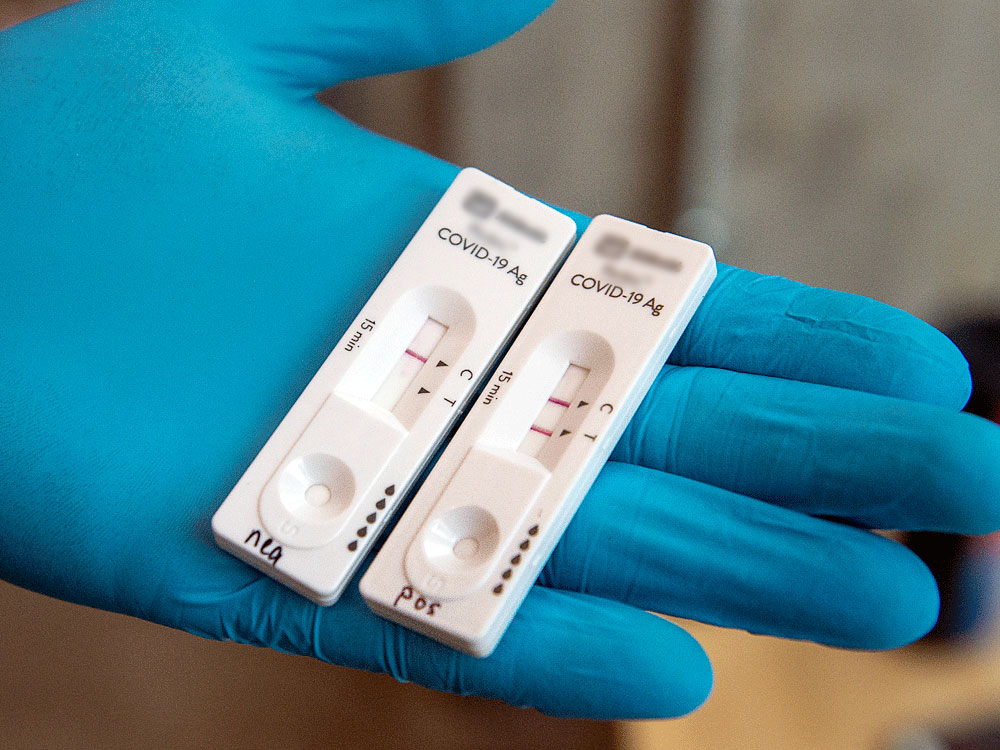
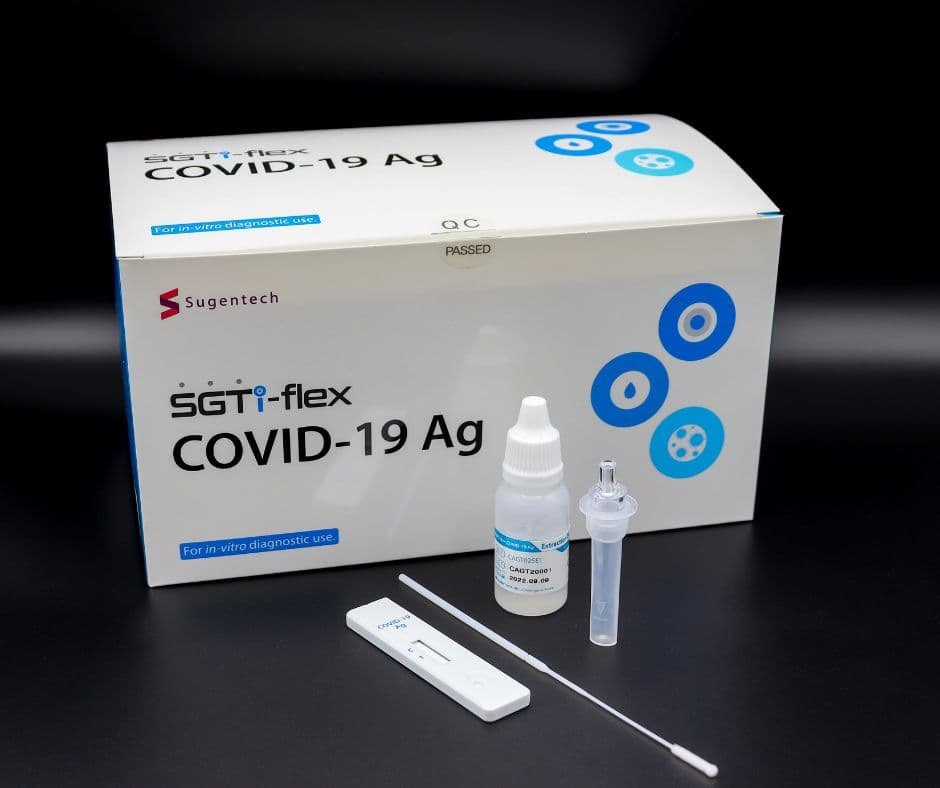
Thủ tục nhập khẩu kit test covid 19
Nội dung bài viết
Thủ tục nhập khẩu kit test covid 19 hay còn gọi là sinh phẩm xét nghiệm chuẩn đoán covid 19 thì phải thực hiện theo hướng dẫn của Nghị định 169/2018/NĐ- CP như các mặt hàng thiết bị y tế khác.
Trong tình thế nguy kịch của dịch Covid 19, nhiều tổ chức, cá nhân, doanh nghiệp có mục đích nhập khẩu kit test Covid 19 nhằm phục vụ nhu cầu xét nghiệm của các cơ sở y tế trên địa bàn cả nước.
Bộ Y tế khuyến khích và ủng hộ các đơn vị nghiên cứu sản xuất và nhập khẩu, tài trợ, viện trợ các trang thiết bị y tế, sinh phẩm chuẩn đoán in vitro phục vụ chuẩn đoán virus SARS-CoV-2 gây dịch bệnh covid 19 có chất lượng đảm bảo cung ứng đủ cho nhu cầu xét nghiệm như hóa chất sử dụng cùng máy PCR, khay thử / que test nhanh,…(bộ kit test covid 19).
Vậy thủ tục nhập khẩu kit test Covid 19 được tiến hành như thế nào? Cùng TTHQSaiGon tìm hiểu qua bài viết sau đây!
Căn cứ pháp lý nhập khẩu kit test covid 19
- Nghị định 36/2016/NĐ-CP về Quản lý trang thiết bị y tế
- Nghị định 169/2018/NĐ- CP ngày 31/12/2018 của Chính phủ sửa đổi bổ sung một số điều của Nghị định 36/2016/NĐ-CP ngày 15/5/2016 của Chính phủ về quản lý trang thiết bị y tế
- Thông tư 30/2015/TT-BYT ngày 12/10/2015 của Bộ Y tế về việc nhập khẩu trang thiết bị y tế
- Thông tư 47/2010/TT-BYT ngày 29/12/2010 của Bộ Y tế hướng dẫn hoạt động xuất khẩu, nhập khẩu thuốc và bao bì tiếp xúc trực tiếp với thuốc phần sinh phẩm chẩn đoán in vitro
- Công văn số 1592/BYT-TB-CT Về việc sản xuất, nhập khẩu trang thiết bị y tế/ sinh phẩm chẩn đoán in vitro chẩn đoán virus Corona (SARS-Cov-2)
Bộ kit test Covid 19 là gì?
Bộ kit test Covid 19 có thể được coi là một loại trang thiết bị y tế và pháp luật Việt Nam đã ban hành những quy định rất cụ thể và rõ ràng về việc nhập khẩu trang thiết bị y tế hay bộ kit test Covid 19 để đáp ứng các nhu cầu về phòng chống và kiểm soát dịch bệnh.
Trang thiết bị y tế là các loại thiết bị, dụng cụ, vật liệu, vật tư cấy ghép, thuốc thử và chất hiệu chuẩn in vitro, phần mềm (software) đáp ứng đồng thời các yêu cầu sau đây:
a) Được sử dụng riêng lẻ hay phối hợp với nhau theo chỉ định của chủ sở hữu trang thiết bị y tế để phục vụ cho con người nhằm một hoặc nhiều mục đích sau đây:
- Chẩn đoán, ngăn ngừa, theo dõi, điều trị và làm giảm nhẹ bệnh tật hoặc bù đắp tổn thương, chấn thương;
- Kiểm tra, thay thế, điều chỉnh hoặc hỗ trợ giải phẫu và quá trình sinh lý;
- Hỗ trợ hoặc duy trì sự sống;
- Kiểm soát sự thụ thai;
- Khử khuẩn trang thiết bị y tế, bao gồm cả hóa chất sử dụng trong quy trình xét nghiệm;
- Cung cấp thông tin cho việc chẩn đoán, theo dõi, điều trị thông qua biện pháp kiểm tra các mẫu vật có nguồn gốc từ cơ thể con người.
b) Không sử dụng cơ chế dược lý, miễn dịch hoặc chuyển hóa trong hoặc trên cơ thể người hoặc nếu có sử dụng các cơ chế này thì chỉ mang tính chất hỗ trợ để đạt mục đích quy định tại điểm a khoản này.”
Chứng từ làm thủ tục nhập khẩu kit test covid 19 (Sinh phẩm xét nghiệm chuẩn đoán covid 19):
Chứng từ nhập khẩu kit test covid 19, để nhập kinh doanh bao gồm:
- Hợp đồng thương mại
- Invoice + packing list
- Bill of lading
- Chứng nhận xuất xứ – Các loại C/O form B, C/O form AK, C/O form D,…
- Test report của bộ kit
- Giất đăng ký kinh doanh
- C/Q – Giấy chứng nhận chất lượng sản phẩm
- Giấy chứng nhận lưu hành tự do của bộ kit test covid 19 (sinh phẩm chuẩn đoán in vitro).
- Tiêu chuẩn thành phần kèm phương pháp kiểm tra chất lượng sản phẩn chuẩn đoán in vitro (bộ kit test covid 19) và phiếu kiểm nghiệm thành phẩm.
- Nhãn sản phẩm (nhãn thiết kế – nhãn chính, nhãn phụ), tờ hướng dẫn sử dụng bộ kit test covid 19: 1 bộ nhãn gốc kèm hướng dẫn sử dụng gốc đang lưu hành thực tế ở nước sản xuất; 2 bộ nhãn dự kiến lưu hành tại Việt Nam kèm tờ hướng dẫn sử dụng bằng tiếng Việt.
- Tài liệu chứng minh số lượng sinh phẩm chuẩn đoán in vitro xin nhập khẩu (bộ kit test covid 19).
- Giấy phép nhập khẩu kit test covid 19 theo thông tư 47 hoặc thông tư 30.
Thời gian để xin giấy phép nhập khẩu kit test covid 19 (sinh phẩm chuẩn đoán in vitro) là 20 ngày tính từ ngày Vụ Trang Thiết Bị Y Tế nhận được bộ hồ sơ hoàn chỉnh.
Thực tế khi tiến hành nhập khẩu bộ kit test Covid 19
Hiện nay, qua rà soát các hồ sơ đề nghị xin giấy phép nhập khẩu, đăng ký lưu hành test kit chẩn đoán SARS-CoV-2, Bộ Y tế nhận thấy phần lớn các test kit chẩn đoán SARS-CoV-2 được nước sản xuất cấp phép để sử dụng trong khẩn cấp, chưa được lưu hành tại nước sản xuất nên giấy chứng nhận lưu hành tự do (CFS) chưa đáp ứng quy định của Điều 10 của Nghị định 69/2018/NĐ-CP ngày 15/5/2018 của Chính phủ.
Nghị định 69 của Chính phủ quy định chi tiết một số điều của Luật Quản lý Ngoại thương (CFS thê hiện sản phâm được sản xuất và lưu hành tại nước sản xuất hoặc nước cấp CFS) và các giấy tờ pháp lý trong hồ sơ chưa được hợp pháp hóa lãnh sự theo quy định. Để đảm bảo có thể có sản phẩm có chất lượng kịp thời đáp ứng nhu cầu xét nghiệm SARS-CoV-2 hiện nay, Bộ Y tế đề nghị các đơn vị:
Trường hợp các sản phẩm CFS thể hiện sản phẩm được lưu hành tại nước sản xuất hoặc nước cấp CFS, công ty được phép nhập khẩu một số lượng mẫu để đánh giá thử nghiệm tại đơn vị kiểm định chất lượng do Bộ Y tế chỉ định. Trên cơ sở kết quả đánh giá của đơn vị kiểm định chất lượng và hồ sơ đề nghị nhập khẩu của đơn vị, Bộ Y tế sẽ cấp nhanh giấy phép nhập khẩu để đơn vị nhập khẩu.
Trường hợp giấy tờ pháp lý trong hồ sơ nhập khẩu chưa hợp pháp hóa lãnh sự: đề nghị đơn vị có công văn chịu trách nhiệm về tính xác thực, cam kết thời gian cung cấp bản họp pháp hóa lãnh sự và đồng thời phải cung cấp đường link tra cứu giấy phép hoặc liên hệ của cơ quan cấp phép đê Bộ Y tế kiểm tra tính xác thực của các giấy tờ chưa được hợp pháp hóa lãnh sự. Tất cả các test kit trên đều được đơn vị kiểm định chất lượng của Bộ Y tế kiểm tra trước khi đưa ra sử dụng sàng lọc, khẳng định…
Các trường hợp được phép cấp nhanh số lưu hành
Các trường hợp được phép cấp nhanh số lưu hành được quy định tại điều 29 nghị định 98/2021/NĐ-CP bao gồm các trường hợp sau:
Điều 29. Các hình thức đăng ký lưu hành
Cấp nhanh số lưu hành mới đối với trang thiết bị y tế thuộc một trong các trường hợp sau đây:
a) Đã được một trong các tổ chức hoặc nước sau cấp giấy chứng nhận lưu hành tự do (Certificate of Free Sale) hoặc giấy chứng nhận lưu hành (Market Authorization) (sau đây viết tắt là giấy lưu hành):
- Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) – Mỹ;
- Cục Quản lý hàng hóa trị liệu (TGA) – Úc;
- Cơ quan quản lý y tế Canada (Health Canada);
- Bộ Y tế, Lao động và Phúc lợi Nhật Bản (MHLW) hoặc Cơ quan Dược phẩm và Thiết bị y tế (PMDA) – Nhật Bản, các nước thành viên EU, Anh, Thụy Sỹ;
- Cục Quản lý sản phẩm y tế quốc gia cấp trung ương (National Medical Products Administration – NMPA) – Trung Quốc;
- Bộ An toàn thực phẩm và dược phẩm (Ministry of Food & Drug Safety – MFDS) – Hàn Quốc hoặc thuộc danh sách các tổ chức cấp giấy lưu hành được cơ quan có thẩm quyền của Việt Nam công nhận (sau đây viết tắt là nước tham chiếu);
b) Đã được cấp Giấy phép nhập khẩu hoặc số lưu hành hoặc Giấy chứng nhận đăng ký lưu hành theo hình thức thương mại tại Việt Nam, trừ các trường hợp đã bị thu hồi trước ngày Nghị định này có hiệu lực;
Hồ sơ xin cấp nhanh số lưu hành
Hồ sơ đề nghị cấp mới số lưu hành đối với trang thiết bị y tế thuộc trường hợp cấp nhanh quy định tại khoản 2 Điều 29 như sau:
a) Văn bản đề nghị cấp mới số lưu hành.
b) Giấy chứng nhận đạt tiêu chuẩn quản lý chất lượng ISO 13845 còn hiệu lực tại thời điểm nộp hồ sơ; Giấy ủy quyền của chủ sở hữu trang thiết bị y tế cho cơ sở thực hiện việc đăng ký lưu hành còn hiệu lực tại thời điểm nộp hồ sơ; Giấy xác nhận đủ điều kiện bảo hành do chủ sở hữu trang thiết bị y tế cấp, trừ trường hợp trang thiết bị y tế sử dụng một lần theo quy định của chủ sở hữu trang thiết bị y tế hoặc có tài liệu chứng minh không có chế độ bảo hành
c) Giấy lưu hành được cấp bởi một trong các nước tham chiếu đối với trường hợp quy định tại điểm a khoản 2 Điều 29 Nghị định này.
d) Giấy lưu hành đối với trang thiết bị y tế nhập khẩu và Giấy phép nhập khẩu hoặc Số lưu hành hoặc Giấy chứng nhận đăng ký lưu hành đối với trường hợp quy định tại điểm b khoản 2 Điều 29 Nghị định này.
đ) Giấy chứng nhận đánh giá chất lượng do cơ quan có thẩm quyền của Việt Nam cấp đối với trang thiết bị y tế chẩn đoán in vitro, trừ các trường hợp sau:
- Thuộc danh mục A, B phụ lục 2 Hiệp định trang thiết bị y tế chẩn đoán in vitro tại Châu Âu và đã được cấp giấy chứng nhận lưu hành tự do (Certificate of Free Sale) của một trong các nước thuộc thành viên EU, Anh, Thụy Sỹ;
- Thuộc danh mục A, B phụ lục 2 Hiệp định trang thiết bị y tế chẩn đoán in vitro tại Châu Âu và đã được cấp giấy chứng nhận lưu hành (Market Authorization) của một trong các nước tham chiếu;
- Không thuộc danh mục A, B phụ lục 2 Hiệp định trang thiết bị y tế chẩn đoán in vitro tại Châu Âu nhưng đã được cấp giấy chứng nhận lưu hành (Market Authorization) của một trong các nước tham chiếu;
- Thuộc danh sách do Bộ trưởng Bộ Y tế công bố.
e) Hồ sơ CSDT (áp dụng từ 01/01/2023 trước đó thì cung cấp hồ sơ sau đây)
- Tài liệu mô tả tóm tắt kỹ thuật trang thiết bị y tế bằng tiếng Việt, kèm theo tài liệu kỹ thuật mô tả chức năng, thông số kỹ thuật của trang thiết bị y tế do chủ sở hữu trang thiết bị y tế ban hành.
- Tài liệu hướng dẫn sử dụng của trang thiết bị y tế. Nộp bản bằng tiếng Việt có xác nhận của tổ chức đề nghị cấp số lưu hành, kèm theo bản gốc bằng tiếng Anh do chủ sở hữu trang thiết bị y tế ban hành đối với trang thiết bị y tế nhập khẩu.
- Mẫu nhãn sẽ sử dụng khi lưu hành tại Việt Nam của trang thiết bị y tế.
Đơn vị kiểm định/ kiểm tra chất lượng bộ kit test covid 19 (sinh phẩn chuẩn đoán in vitro), trang thiết bị Y tế xét nghiệm virus Corona (SAR-CoV-2).
- Viện vệ sinh dịch tể Trung Ương
- Viện Pasteur thành phố HCM
- Viện Pasteur Nha Trang
- Viện kiểm định quốc gia vaccine và sinh phẩm y tế.
Thuế nhập khẩu kit test nhanh covid 19 (sinh phẩm chuẩn đoán vi intro)
Mã HS code bộ kít test covid 19 các bạn có thể tham khảo mã sau:
- Mã hs bộ kit test nhanh covid 19: 382200 hoặc 300215
- Dụng cụ chuẩn đoán covid 19: 902780
Thuế nhập khẩu kit test nhanh covid 19 )%
Thuế VAT bộ kit test nhanh covid 19: 5%
Các bạn cần hỗ trợ làm hồ sơ giấy tờ về Thiết bị y tế hay liên hệ ngay 0949635389 để được tư vấn tận tình và báo giá nhanh nhé!
TTHQSaiGon cung cấp các dịch vụ về nhập khẩu thiết Trang thiết bị y tế:
- Xin giấy phép nhập khẩu thiết bị y tế
- Phân loại thiết bị y tế loại A,B,C,D
- Xin đăng ký lưu hành thiết bị y tế loại B,C,D
- Xin công bố loại A
- vận chuyển EXW, FOB, khai hải quan trọn gói
- Thủ tục tạm nhập tái xuất, tạm xuất tái nhập hàng thiết bị y tế
- Công bố mỹ phẩm
Xem thêm các thông tin mới về xuất nhập khẩu, chính sách xuất khẩu hàng, nhập khẩu hàng qua fanpage hay group facebook XUẤT NHẬP KHẨU HCM nhé:
Fanpage: https://www.facebook.com/xuatnhapkhauhcm/
Group: https://www.facebook.com/groups/1073402229658531/
Nguồn: Khắc – TTHQSaiGon
Liên hệ:
Skype: khac5579
SĐT: 0949 63 53 89 / 0348 0000 69
Email: tthqsaigon@tthqsaigon.net
Where there is a will, there is a way.!!!
Liên quan:
THỦ TỤC NHẬP KHẨU MỰC NỒI XOONG CHẢO
THỦ TỤC NHẬP KHẨU MỰC ỐNG ĐÔNG LẠNH
THỦ TỤC NHẬP KHẨU VẢI KHÔNG DỆT
THỦ TỤC NHẬP KHẨU PHỤ TÙNG Ô TÔ